A tabela periódica dos elementos químicos foi proposta há 150 anos por Dmitri Mendeleev (1834-1907). O químico de origem russa agrupou os elementos em famílias, de acordo com as semelhanças de propriedades físicas e químicas, chegando mesmo a prever a existência de outros não conhecidos à época, com base nas suas propriedades.
Desde então, muitos elementos químicos foram descobertos e outros criados em laboratório, chegando aos 118 conhecidos atualmente. A forma de apresentação da tabela também mudou, passando do agrupamento horizontal, originalmente proposto por Mendeleev, para o agrupamento vertical das famílias de elementos, forma utilizada atualmente.

Dos elementos que compõem a tabela hoje em dia, 26 são produzidos artificialmente pela humanidade, na busca por conhecer os limites da matéria e da estrutura do átomo. São os elementos transurânicos, ou mais pesados que o urânio, que são produzidos em laboratório por reações nucleares controladas. Os outros 92 são encontrados na natureza em diferentes graus de abundância em nosso planeta.
Recentemente, cientistas começaram a esboçar a tabela periódica dos elementos químicos em extinção. Mas como pode um elemento químico ser extinto? Eles são inanimados e “na natureza nada se cria, nada se perde, tudo se transforma”, como dizia o pai da química moderna, o químico francês Antoine Lavoisier (1743-1794).
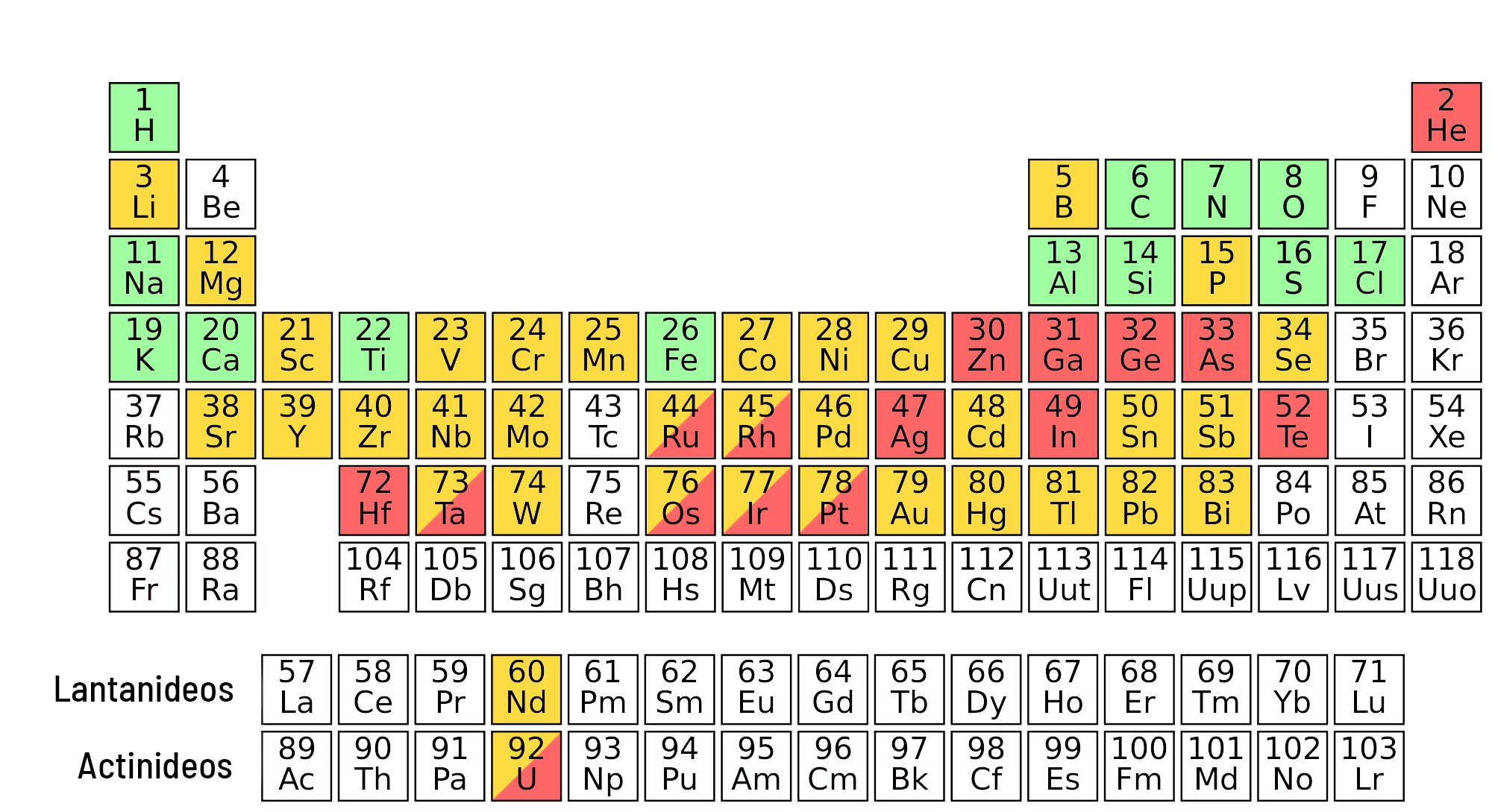
Essa nova tabela mostra os elementos que estão em risco iminente nos próximos 100 anos (em vermelho), além daqueles que correm sérios riscos em futuro próximo devido ao seu uso crescente (em amarelo). Há, ainda, os que se encontram em uma posição intermediária, podendo rapidamente entrar na lista dos mais ameaçados (em vermelho e amarelo).
Para entendermos por que vários elementos da tabela periódica correm risco de extinção em nosso planeta, antes precisamos compreender como eles são formados no universo e como chegaram à Terra. Isso inclui um passeio pela astronomia, pela física e pela origem dos tempos.
A teoria mais aceita atualmente para a origem do universo é a do Big Bang. No início, toda a matéria do universo era concentrada em um único ponto e, a partir de uma explosão, essa matéria começou a ser espalhada. Nos instantes iniciais, se formaram as partículas subatômicas, como prótons, nêutrons e elétrons; na sequência, formaram-se os átomos e depois as moléculas, que deram origem às estrelas, planetas e demais corpos celestes .

As estrelas são as verdadeiras fábricas de elementos químicos. Elas transformam o hidrogênio, o elemento mais simples que existe, em hélio, por meio de reações nucleares complexas. Posteriormente, o hélio formado dá origem a outros elementos, como o carbono, o nitrogênio e o oxigênio, chegando até ao ferro. Todos esses processos ocorrem por meio de reações nucleares de alta complexidade.
Já os elementos mais pesados que o ferro só se formam em condições particulares, sobretudo nos instantes finais da vida de uma estrela. Um desses eventos é a supernova, uma explosão intensa e brilhante que marca a morte de estrelas com massas maiores que oito vezes a do nosso Sol. As reações nucleares que ocorrem nesse processo originam esses elementos mais pesados que o ferro, que, após a explosão, são espalhados no universo.
O nosso sistema solar foi formado há cerca de 4 bilhões de anos pela agregação de material oriundo da explosão de alguma supernova. No início, a Terra recém-formada era constantemente bombardeada por meteoritos e material estelar, os quais trouxeram todos os elementos químicos que encontramos no nosso planeta até os dias de hoje. Ou seja, praticamente toda a matéria que existe na Terra remete à sua formação, há cerca de 4 bilhões de anos.
Se olharmos a tabela periódica dos elementos químicos em extinção, sobretudo aqueles com sérios riscos nos próximos 100 anos, veremos que eles são mais pesados que o ferro, com exceção do hélio. Isso pode ser explicado, de certa forma, pela relativa escassez desses elementos no universo, já que são formados apenas nos instantes finais da vida de algumas estrelas. Estima-se que cerca de 75% da matéria do universo seja hidrogênio, o elemento mais simples da tabela periódica; o hélio corresponde a 23%, enquanto os demais elementos químicos somam os 2% restantes.
A ação humana é determinante para a escassez desses elementos. Seu uso crescente, sobretudo em dispositivos eletrônicos, como os aparelhos celulares, vem levando a uma rápida depleção das reservas conhecidas, o que ameaça a existência comercial desses elementos na Terra na forma que os conhecemos hoje em dia. Os elementos químicos não vão acabar, ou se extinguir no sentido exato da palavra; seu uso irracional e crescente pode levar ao esgotamento das reservas comerciais, já que muitos são encontrados em pequenas proporções em nosso planeta.
O hélio é um caso à parte, pois praticamente todo átomo desse gás nobre na Terra é formado pela decomposição de minerais radiativos, como o urânio. Por ser muito leve, o hélio pode escapar da atmosfera da Terra e ir para o espaço sideral, sendo relativamente raro no nosso planeta. O uso em dirigíveis, sistemas de respiração submarinos e, sobretudo, em ímãs supercondutores agrava o problema, pois aumenta a demanda por esse elemento.
O gálio e o arsênio estão em extinção devido ao uso em semicondutores e lâmpadas de LED (sigla em inglês para diodo emissor de luz). Os dois elementos dão origem a um diodo que emite luz vermelha.
O índio é um dos principais elementos que compõem as telas sensíveis ao toque de aparelhos eletrônicos, sobretudo os telefones celulares. Ele forma o óxido de índio e estanho (conhecido pela sigla em inglês ITO), um composto condutor e transparente usado para produzir um filme delgado que, devido às suas propriedades condutoras, faz o mecanismo de sensibilidade ao toque funcionar sem gerar opacidade na tela. As quantidades de índio em cada aparelho celular são muito pequenas, apenas alguns miligramas. No entanto, com o uso crescente de dispositivos tecnológicos, o índio corre sério risco de extinção nos próximos 100 anos.
O germânio é muito utilizado em lentes e fibras óticas e também tem aplicações em circuitos eletrônicos, como semicondutor. Já o háfnio é considerado um dos elementos mais ameaçados. Suas reservas são limitadas, e ele é matéria-prima para componentes de turbinas de aviões, bem como de reatores nucleares, para controlar o processo de fissão. O telúrio é usado em painéis solares, CDs, DVDs e em aços especiais.
A prata e o zinco são outros que correm risco de extinção nos próximos anos. Estima-se que cerca de 80% das reservas de prata já foram exploradas; há um risco de extinção comercial desse elemento em um período de 25 anos. A ameaça à prata não se deve ao seu uso em joias e ornamentos decorativos, mas sobretudo ao emprego em dispositivos eletrônicos. Devido à sua alta condutividade elétrica e excelente resistência química, a prata tem sido muito utilizada em circuitos eletrônicos de celulares, computadores, fones de ouvido, entre outros. O material também tem aplicações cada vez mais crescentes como catalisador em processos químicos.
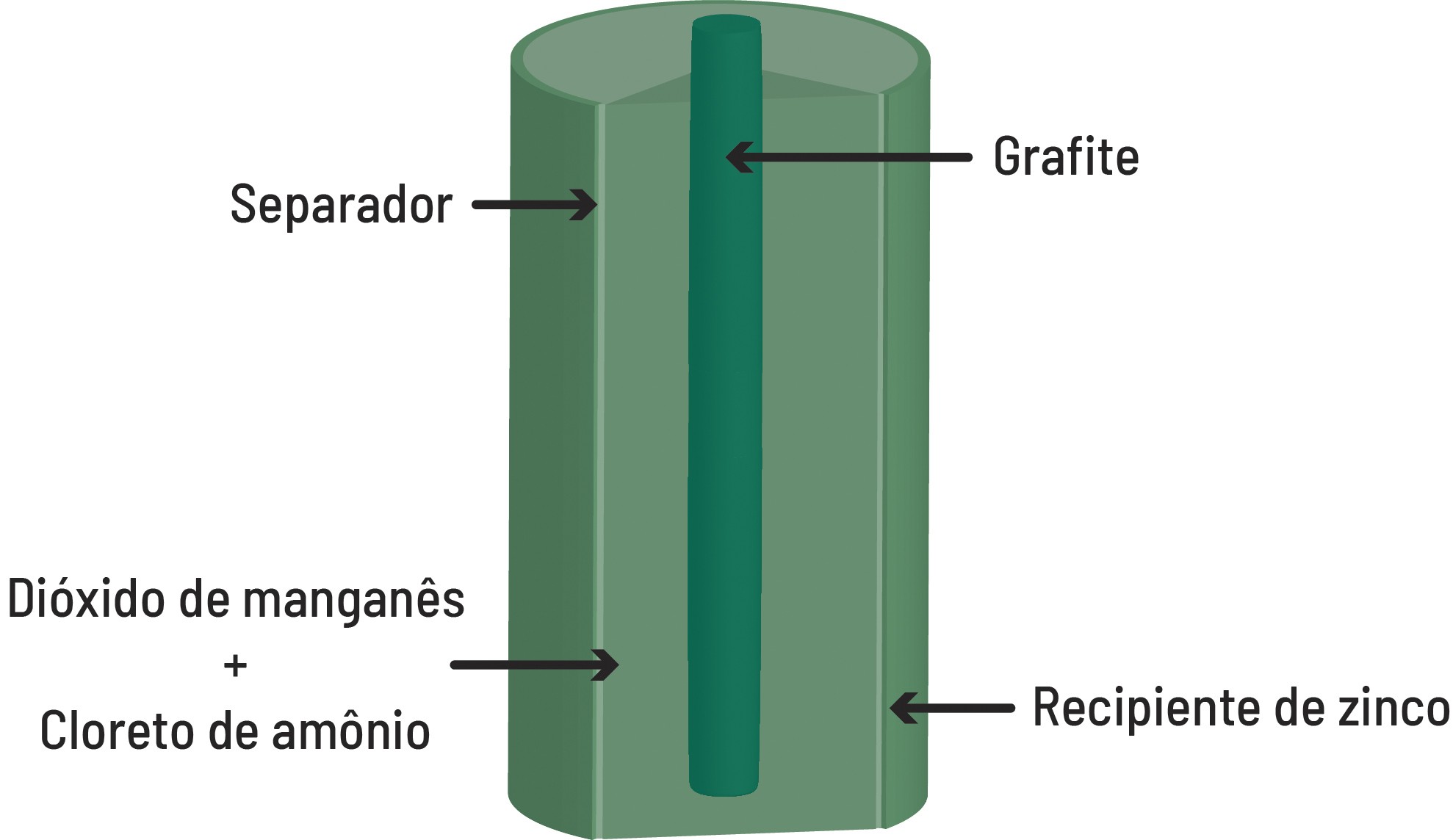
O zinco é outro elemento que vem sendo usado pelos humanos há muitos anos, desde a pré-história. Apesar de ser o 24o elemento mais abundante na crosta terrestre, suas inúmeras aplicações o colocam na lista dos elementos mais ameaçados. É muito utilizado no processo de galvanização do aço, para proteção contra corrosão, e na produção de pilhas e baterias, nas quais é aproveitado como polo negativo. Além dessas aplicações, o zinco também participa do processo de vulcanização da borracha, que confere a ela maior força, elasticidade e resistência à temperatura. Algumas tintas também contêm zinco em sua formulação.

A pergunta que fica é: podemos reverter esse quadro assustador e manter nosso padrão de vida, desfrutando de todas as comodidades tecnológicas? A resposta é sim, mas será preciso mudar nosso padrão de consumo e produção de bens.
Os smartphones revolucionaram nosso modo de vida, permitindo uma maior comunicação entre as pessoas e um acesso mais rápido e prático à informação. Entretanto, precisamos reconhecer que os recursos naturais são finitos e precisam ser usados com extrema prudência.
Atualmente, vivemos na chamada economia linear. Os recursos minerais são explorados, transformados em produtos, que são vendidos ao consumidor e, depois, descartados e substituídos por outros, de geração tecnológica mais avançada. Esse ciclo gera um passivo ambiental enorme. Praticamente nada no produto descartado é reaproveitado, levando à depleção dos recursos naturais. Tudo para manter em alta o processo produtivo e a lógica de empresas e consumidores

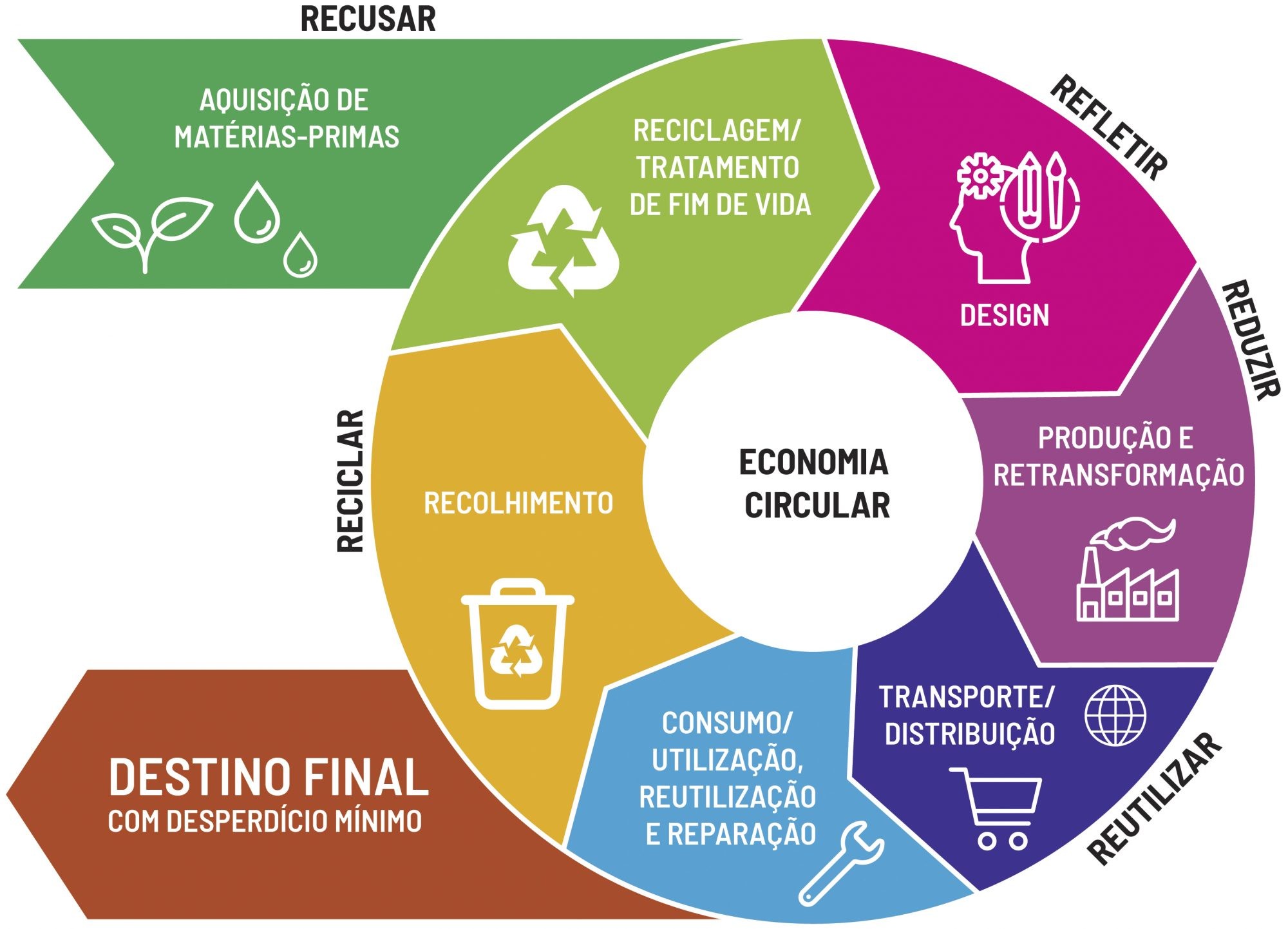
É preciso que a sociedade evolua para a chamada economia circular, na qual os rejeitos e descartes tornam-se matéria-prima para a produção de novos bens de consumo. Isso gera menos problemas ambientais e contribui com a exploração responsável dos recursos naturais e a maior sustentabilidade do processo produtivo. Há também grande impacto econômico, à medida que atividades de coleta, reciclagem e reutilização geram inúmeros empregos.
Nossa sociedade se acostumou a consumir sem pensar no amanhã, sem imaginar que todos os recursos naturais são finitos e podem não existir mais da forma como os conhecemos em um futuro não tão distante.
Será necessária uma reeducação, uma mudança de mentalidade, que englobe produtores, consumidores e governos. Será preciso investir em reciclagem, reutilização e reaproveitamento para que um ciclo virtuoso se forme.
As empresas ganharão por manterem seu portfólio de produtos e inovação, fundamental em um mercado caracterizado por novos lançamentos e apelos de marketing. Os consumidores se beneficiarão pela oferta crescente de novos produtos e redução de preços, pois, com a depleção dos recursos naturais, a pressão sobre o custo das matérias-primas irá crescer. Os governos poderão se beneficiar com a criação de novos impostos, principalmente sobre a atividade de reciclagem e reutilização, e evitarão gastos públicos com aterros, lixões e recuperação de áreas poluídas, economizando recursos para aplicação em áreas mais importantes para a população, como educação, saúde, habitação e segurança. Ou seja: é um bom negócio para todos reciclar, reutilizar e reaproveitar para não faltar.
Claudio J. A. Mota
Instituto e Escola de Química,
Universidade Federal do Rio de Janeiro

Eles são usados em aeroportos para testes de triagem de suspeitos de carregarem ou terem tido contato com explosivos. Mas esses equipamentos são totalmente confiáveis? Estudo de um grupo de pesquisadores brasileiros atacou essa questão. E a resposta foi surpreendente.

O que aquela refeição que acaba queimada numa panela e o envelhecimento têm a ver? Ao longo da vida, nosso organismo também sofre uma ‘fervura’ silenciosa que pode causar várias doenças. Boa notícia: a ciência já é capaz de entender e diminuir essa ‘chama’.

Cientistas têm o dever de corrigir suas publicações sempre que necessário, mas essa prática ainda carrega um estigma. Aos poucos, essa cultura está mudando: as correções, principalmente, quando voluntárias e transparentes, estão sendo cada vez mais valorizadas

Os fenômenos do mundo macroscópico, em que vivemos, são bem diferentes daqueles que ocorrem com átomos e moléculas. Há uma sutil (e misteriosa) fronteira entre esses dois mundos, apresentada neste artigo, que comemora o Ano Internacional da Ciência e das Tecnologias Quânticas

Avaliações internacionais mostram que o conhecimento de matemática dos alunos brasileiros é baixíssimo no fim do ensino básico. Outro fato preocupante: as altas taxas de desistência nas graduações em matemática. Um novo exame pretende enfrentar o problema.

Seu prato de comida é bem mais do que aquilo que está nele. Ele reflete uma cadeia complexa de atividades – muitas delas, ainda prejudiciais para o meio ambiente. Mas a ciência, de forma interdisciplinar, já está mobilizada para resolver esses problemas.

O fenômeno – adaptação evolutiva crucial para proteger, de respostas imunes prejudiciais, órgãos e tecidos vitais, como olhos, placenta, cérebro e testículos – abre novas possibilidades para tratamentos mais eficazes contra o câncer e condições que envolvem o sistema imunitário.

Para entender melhor a complexidade e o desafio existencial que essa nova era significa para todas as espécies, é preciso rever enquadramentos disciplinares rígidos e mais tradicionais: geólogos, cientistas climáticos e cientistas sociais precisam trabalhar em conjunto
| Cookie | Duração | Descrição |
|---|---|---|
| cookielawinfo-checkbox-analytics | 11 months | This cookie is set by GDPR Cookie Consent plugin. The cookie is used to store the user consent for the cookies in the category "Analytics". |
| cookielawinfo-checkbox-functional | 11 months | The cookie is set by GDPR cookie consent to record the user consent for the cookies in the category "Functional". |
| cookielawinfo-checkbox-necessary | 11 months | This cookie is set by GDPR Cookie Consent plugin. The cookies is used to store the user consent for the cookies in the category "Necessary". |
| cookielawinfo-checkbox-others | 11 months | This cookie is set by GDPR Cookie Consent plugin. The cookie is used to store the user consent for the cookies in the category "Other. |
| cookielawinfo-checkbox-performance | 11 months | This cookie is set by GDPR Cookie Consent plugin. The cookie is used to store the user consent for the cookies in the category "Performance". |
| viewed_cookie_policy | 11 months | The cookie is set by the GDPR Cookie Consent plugin and is used to store whether or not user has consented to the use of cookies. It does not store any personal data. |
