Segundo a Organização das Nações Unidas (ONU), 15 milhões de brasileiros que moram em áreas urbanas e 2,3 milhões de moradores rurais não têm acesso a fontes seguras de água para suas necessidades domésticas e pessoais. A má higienização causada pela falta de água potável é um fator de maior vulnerabilidade para doenças adquiridas através do consumo de alimentos e água contaminados. Esse é o caso da toxoplasmose, prevalente em todo Brasil.
Embora as autoridades não a reconheçam como doença negligenciada, o país ocupa o topo da lista de surtos e casos de toxoplasmose no mundo. Entre 2010 e 2018, foram registrados 14 surtos no Brasil, correspondendo a 56% dos 25 notificados nos últimos 50 anos.
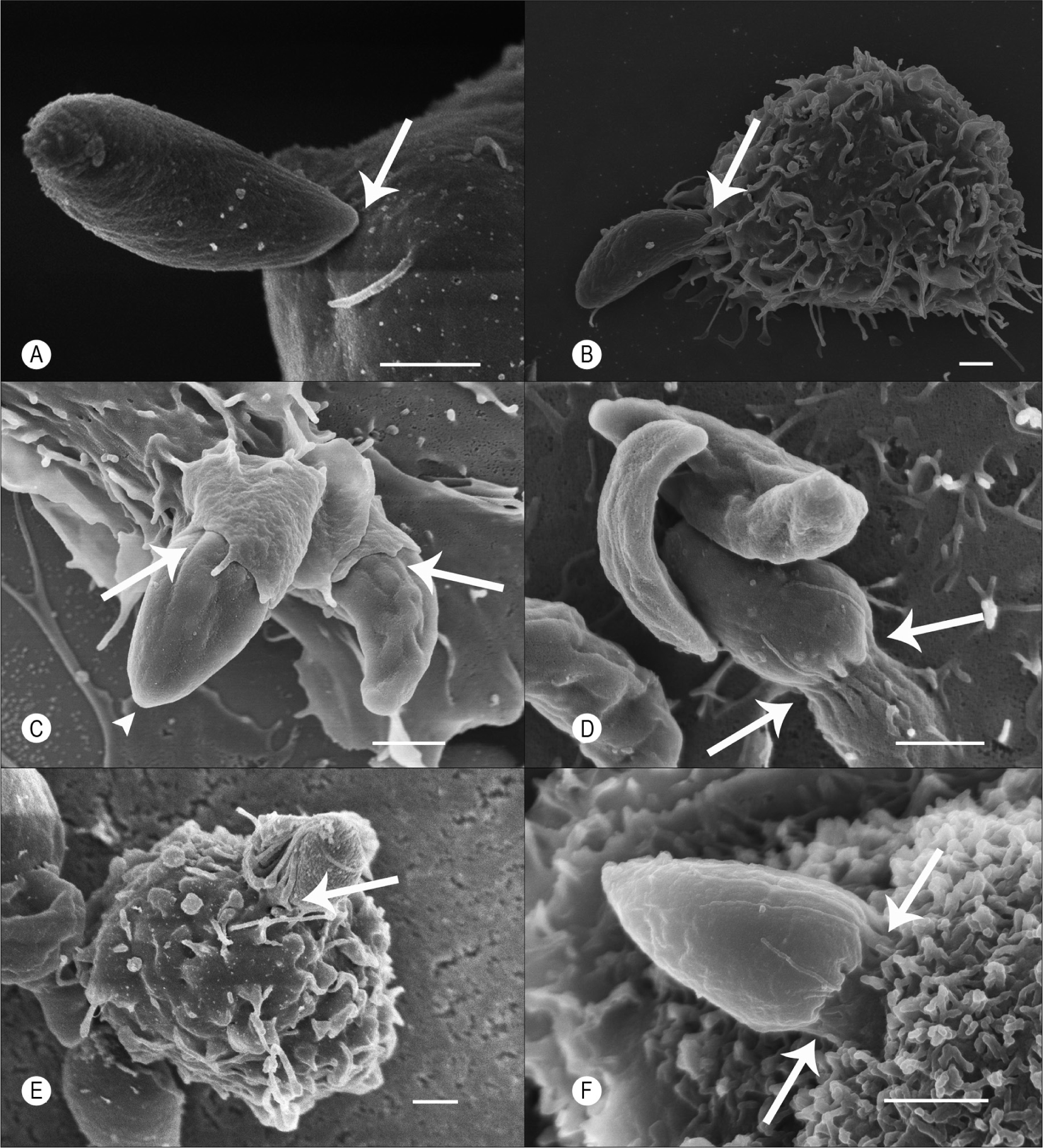
Além de ser transmitido por via oral, o parasita Toxoplasma gondii é capaz de ultrapassar barreiras importantes do nosso organismo, como a placenta. Por isso, pode ser transmitido para o feto em desenvolvimento se a infecção ocorreu durante a gestação – é a denominada toxoplasmose congênita.
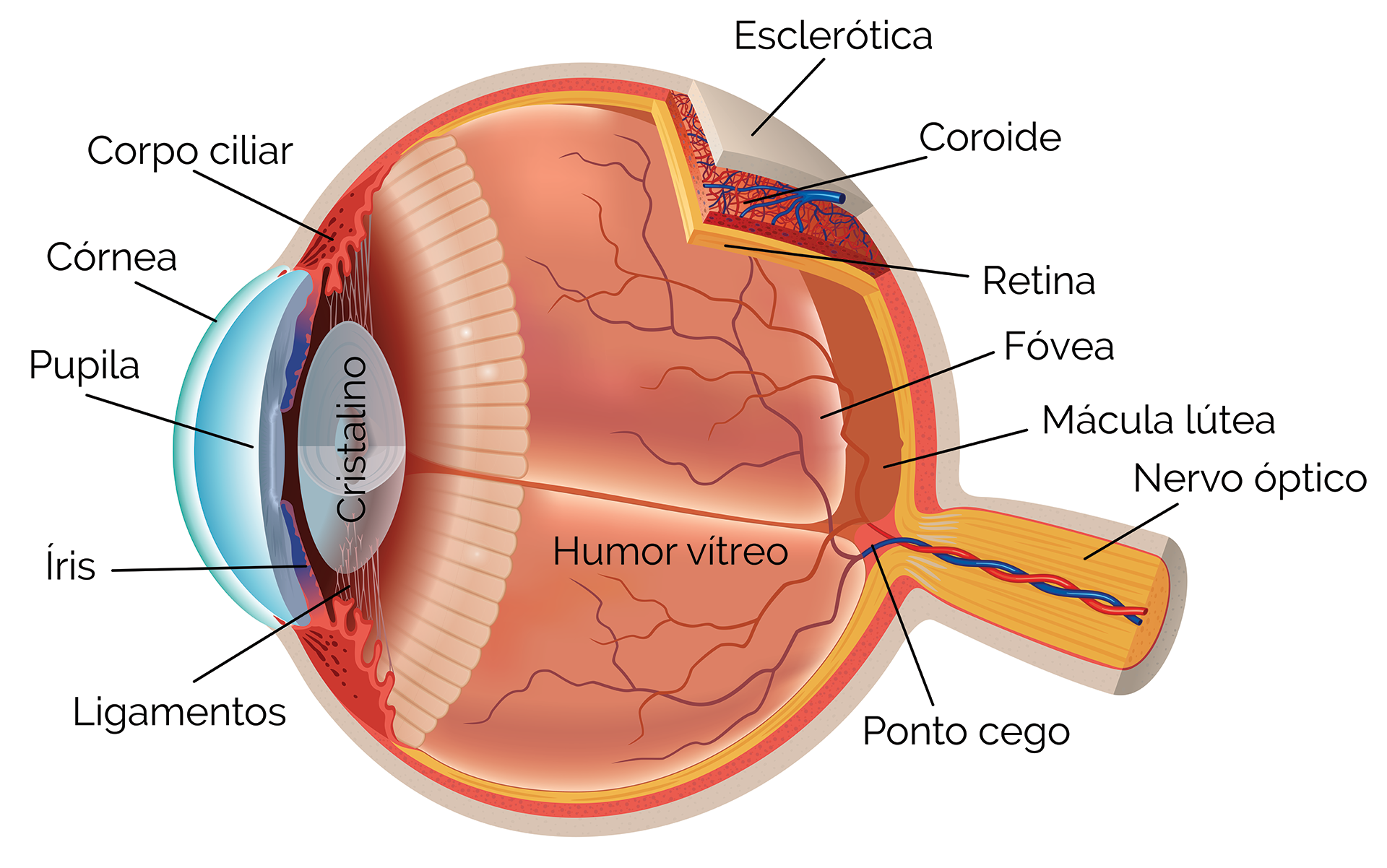
Nos bebês, a toxoplasmose congênita pode ser assintomática, além de provocar sintomas graves, como atraso no desenvolvimento, cegueira, hidrocefalia. Dentre os fatores que contribuem para a gravidade das consequências da infecção, está o período da gestação em que o feto foi infectado. Os casos de aborto são mais comuns nas infecções adquiridas no primeiro trimestre de gravidez.
Embora a maioria dos recém-nascidos com toxoplasmose congênita sejam assintomáticos, os sinais da tríade clássica da doença – retinocoroidite, calcificação intracraniana e hidrocefalia – ocorrem em mais de 10% dos indivíduos desse grupo. Há outros casos também em que a doença se manifesta com sinais não específicos de infecção aguda, como convulsões, aumento do baço e fígado, febre, anemia, icterícia, linfadenopatia, entre outros.
Alguns dos recém-nascidos desse grupo podem desenvolver sintomas clínicos e deficiências na vida adulta, afetando, sobretudo, a visão. No Brasil, a principal consequência da infecção nos fetos é a formação de lesões oculares, que corresponde a aproximadamente 80% dos casos clínicos de toxoplasmose gestacional registrados.